Les levures

Levure chimique, levure de boulanger... Quelles sont les différences et comment ça marche ?
Date de publication : 27/09/15
Le principe des levures
Le principe des levures est de produire un gaz. Ce gaz est emprisonné dans la pâte au cours de la cuisson. Le gaz est un état dans lequel la matière prend beaucoup plus de place que le liquide, ce qui produit une expansion de (fait lever) la pâte. Les bulles qui restent emprisonnées apportent du moelleux au futur pain ou gâteau.
Les levures sont soit « chimiques » soit « naturelles » (comme la levure de boulanger). Les levures chimiques sont des mélanges de solides qui produisent du gaz strictement par réaction chimique, alors que la levure de boulanger est un microorganisme qui produit du gaz. Dans les deux cas, c’est le dioxyde de carbone (CO2) qui est le principal gaz produit par les levures.
A l’intérieur des levures chimiques1
Les levures chimiques libèrent du CO2 lors de réactions chimiques. Bien entendu, ces réactions ne doivent pas se produire dans le sachet ! Une fois mélangées à la pâte, elles doivent permettre une production de gaz au bon moment. En effet, si la réaction a lieu au moment de mélanger la levure à la pâte, les bulles de gaz ne resteront pas dans la pâte liquide bien longtemps : comme le gaz dans de l’eau pétillante. Idem si la libération a lieu une fois la pâte déjà cuite ! C’est pour cela que ces réactions se produisent à une certaine température et en présence d’humidité. Enfin, la levure ne doit pas apporter un goût désagréable. En ça les additifs ajoutés à la levure chimique sont très importants.
La production de CO2
Les produits les plus communs et historiquement utilisés pour les levures chimiques sont le bicarbonate de sodium (NaHCO3), le carbonate d’ammonium ((NH4)2CO3) et bicarbonate d’ammonium (NH4HCO3). Nous allons donc commencer par aborder les réactions qui permettent la libération de CO2 à partir du bicarbonate de sodium. Il en existe : la réaction acido-basique et la décomposition thermique.
Une réaction chimique assez connue consiste à mélanger du vinaigre d’alcool et du bicarbonate de sodium. C’est le mélange d’un acide (vinaigre d’alcool) et d’une base (bicarbonate de sodium) qui est responsable du dégagement gazeux.
Réaction 1 : la réaction acido-basique (voir les expériences)
H+ + NaHCO3 → Na+ + H2O + CO2
Acide + bicarbonate de sodium à sodium + eau + gaz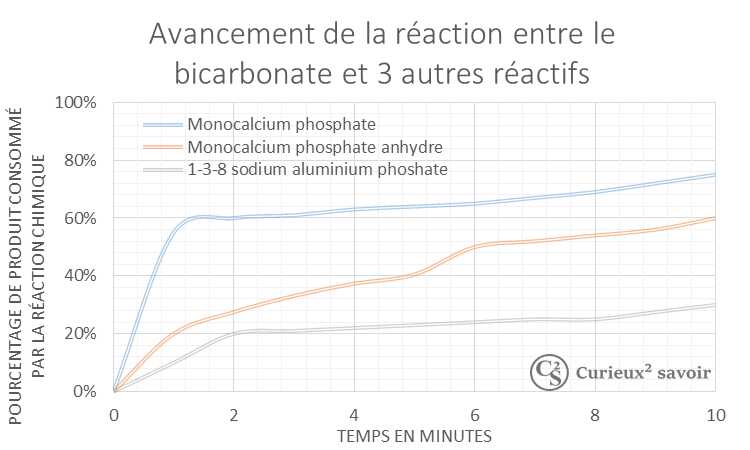
Pour faire cette réaction il faut donc un composé acide. Dans les premiers temps, les gens utilisaient du vinaigre, du jus de citron, de la crème de tartre (bitartrate de potassium) ou encore du lait aigre. Le problème, c’est que la réaction est très rapide avec ces composés ! Si la pâte du gâteau est trop liquide, le gaz reste peu emprisonné et au final le gâteau ne lève pas super-super. Plus tard, les chimistes trouveront d’autres composés acides qui permettent une réaction plus lente.
L’autre réaction est la décomposition par la chaleur. Ici c’est la chaleur qui casse la molécule de bicarbonate de sodium. Cette réaction commence à 30°C mais elle est optimale et la plus rapide à 200°C.
bicarbonate de sodium + chaleur à carbonate de sodium (composés au goût amer) + eau + gaz 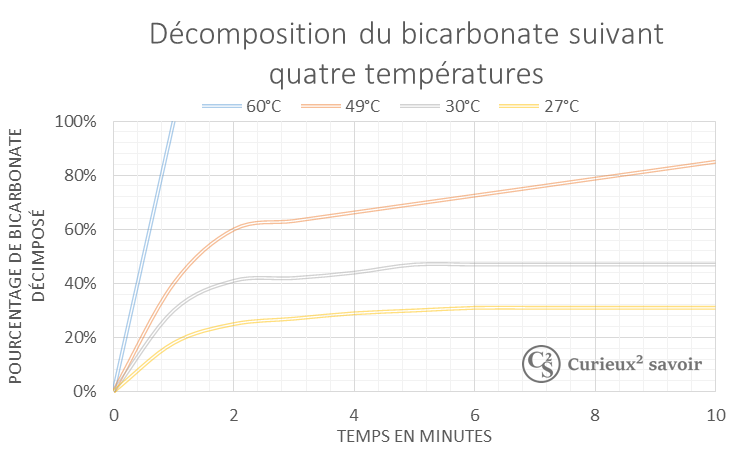
On l’oublie souvent, mais une réaction chimique n’est pas forcément immédiate. Ici 100% du bicarbonate de sodium se décompose en 2 minutes à 60°C, mais seulement 1/5 le serait à 27°C.
Dans les deux cas il y a la production de gaz carbonique qui permet de faire lever la pâte. Si vous avez déjà cuisiné un cake avec du bicarbonate de sodium, vous avez déjà eu cette impression d’un arrière-gout amer ou de « savon ». Ceci est dû à un autre composé produit lors de cette réaction : Na2CO3.
Optimiser le goût et le levage
Pour cela les industriels ont ajouté des acides dans les levures chimiques afin de décomposer le Na2CO3. Le problème est que si on met un acide trop fort, il réagit tout de suite avec le bicarbonate, comme nous venons de le voir pour la première réaction. Il faut donc trouver un acide « cool ». Celui qui se réveille à l’heure qui faut. Pour cela on choisit de acides actifs à partir d’une certaine température ou qui mettent du temps à réagir.
Après 10 minutes, 5 fois plus de bicarbonate de sodium réagit en de mono-calcium phosphate (bleu) comparativement au phosphate d’aluminium (gris).
Les premières levures chimiques contenaient de la poudre de babeurre (une fraction acide du lait). Une recette de grand-mère consiste à ajouter de la crème fraiche à du bicarbonate de sodium pour faire de la levure. Les composés acides du lait vont enlever le goût laissé par les réactions chimiques de levage.
Les composés acides utilisés actuellement sont de la crème de tartre (bitartrate de potassium C4H5KO6), le phosphate monocalcique (CaH2(PO4)2) ou encore le 1-3-8 sodium aluminium phosphate (NaH14Al3(PO4)8·4H2O). Ces composés agissent à basse température et sont plutôt utilisés pour faire la première réaction (la réaction acide). A haute température, d’autres acides prennent le relais et permettent d’inhiber le mauvais goût obtenu après la première réaction. Les sels d’acides actifs à haute température comprennent le sodium aluminium sulfate (NaAl(SO4)2·12H2O), le sodium aluminium phosphate ((NaH14Al3(PO4)8·4H2O et Na3H15Al2(PO4)8) et le pyrophosphate de sodium qui a pour formule Na4P2O7.
Dans certains cas, les produits attirent l’humidité, on ajoute alors de l’amidon de maïs.
 L’infographie
L’infographie
La levure naturelle
La levure de boulanger, la levure de bière et les ferments du vin et du kéfir sont une souche de champignon : Saccharomyces cerevisiae. Cette levure tire son énergie du glucose, et le dégrade en produisant du CO2 et… de l’éthanol (c’est-à-dire de l’alcool) !
Cette réaction n’est rien d’autre que la fermentation alcoolique. Elle intervient quand la levure est à l’abri de l’oxygène, ce qui est le cas à l’intérieur de la pâte !
Levain2
Le levain est un mélange de levures et de bactéries lactiques. Pour faire du levain, il suffit de laisser reposer dans un coin de l’eau mélangée à de la farine. Le mélange capte les levures et bactéries présentes dans l’air, sur les ustensiles utilisés et dans les ingrédients de départ. On créé alors un lupanar à microorganismes en fournissant de la nourriture à gogo et des conditions favorables (température). Tout ce beau monde croît et se multiplie. Ces coopérations collectivistes marxistes dans la nature sont appelées symbioses. Chacun y trouve son compte.
La fermentation des céréales et des farines de céréales est l’un des procédés biotechnologiques des plus anciens. Les Egyptiens faisaient déjà de la bière et du pain ! Au siècle dernier, l’utilisation de farine blanche et de levure de boulanger est devenue la norme pour faire lever le pain. Mais depuis le levain est redevenu à la mode car il a un effet sur la texture du pain et sa saveur. Encore plus impressionnant, le levain permet de réduire l’indice glycémique (il retarde la dégradation de l’amidon en sucre lors de la digestion) et améliore la biodisponibilité des minéraux naturellement présents dans la farine.
Les bactéries lactiques produisent des composés, appelés acides lactique et acétique (le même que celui du vinaigre). Ils acidifient le levain. Ces conditions permettent l’activation et l’activité d’enzymes (sortes de catalyseurs) qui permettent une meilleure digestion du pain2,3.
Phosphoré par : Gontier Adrien, Jaeger Catherine
Mots clefs : levure, bicarbonate






